 07-21-2010
07-21-2010
|
Mã bài: 65271
#11
|
|
VIP ChemVN
Tham gia ngày: Jul 2009
Posts: 581
Thanks: 128
Thanked 828 Times in 447 Posts
Groans: 0
Groaned at 22 Times in 14 Posts
|
Trích:
ở 25oC ,Eo H3AsO4/H3AsO3=0.559 V và Eo I3 -/I- =0.536 V
a) Hãy Viết Pt phản ứng xảy ra giữa các cặp oxi hóa khử trên .
b) với ph bằng bao nhiêu thì phản ứng trên xảy ra theo chiều ngược lại .
c) tính hằng số cân bằng của phản ứng .
Mọi người làm dùm tui nha ^^.
|
Theo tớ thỳ thế này :
a)H3AsO4+3I- +2H+ -->H3AsO3+I3- +H2O
b) Muốn cho phản ứng xảy ra theo chiều ngược lại thì E H3AsO4/H3AsO3 < E I3-/I-.
Chỉ có cặp H3AsO4/H3AsO3
H3AsO4+2H+ +2e-->H3AsO3+H2O
[H3AsO4]=[H3AsO3]=1M.
Do đó ta có :E H3AsO4/H3AsO3
= Eo H3AsO4/H3AsO3-0.059/2*Lg( [H3AsO3]/([H3AsO4][H+]^2))
=0.559-0.059/2*Lg(1/[H+]^2)
=0.059-2*0.059/2*Lg(1/[H+] ).
=0.559-0.059*pH< Eo I3-/I=0.536
-->pH>0.39
Vậy khi pH >0.39 thì phản ứng đổi chiều .
c) Tính hằng số cân bằng của phản ứng trên
K=10^ ( n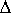 E /0.059 )=6.02 E /0.059 )=6.02
|

|

|



